肿瘤科
CAR-T疗法、TCR-T疗法研发格局
核心提示:
文章目录:
一、T细胞疗法发展历史
二、TCR-T疗法简介
三、CAR-T疗法简介
四、CAR-T疗法的毒性控制
五、T细胞疗法的未来
六、T细胞疗法研发企业
七、小编总结
T细胞疗法发展历史
近年来,T细胞介导的免疫疗法越来越受欢迎,免疫检点抑制剂和CAR-T疗法更是让大药企以及资本趋之若鹜。根据clinical.gov的数据,截至发稿日,全球范围内进行的CAR-T疗法临床研究达到282项。本文主要参考CAR-T疗法大牛“六爷”(Carl H June)的文章,梳理T细胞疗法的历史、现状,同时梳理产业界的竞争格局。
最早成功应用的癌症过继细胞疗法是在1956年,E. Donnall Thomas教授利用双胞胎间的骨髓移植来治疗白血病,避免了移植物抗宿主反应(GVHD),为此与约瑟夫・默里一起获得1990年的诺贝尔生理学或医学奖。不同宿主间的骨髓移植,又经过了十几年的探索,组织相容性抗原配型的研究发现,使得不相关个体间的骨髓移植成为可能,并于1979年在西雅图成功实现了不相关个体间的骨髓移植。直到今天,骨髓移植仍然是许多类型白血病的主要疗法。但骨髓移植不仅价格高昂,而且仍然有很大风险发生GVHD,很多时候甚至是致命的。
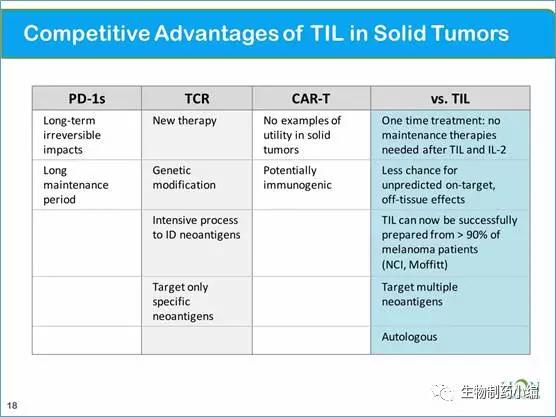
2002年,美国国家癌症研究所(NCI)的Steven Rosenberg教授从癌症患者的肿瘤组织中提取了肿瘤浸润性淋巴细胞(TIL),体外扩充培养后回输到患者体内,治疗转移性黑色素瘤。TIL疗法有很多限制:不是所有患者的肿瘤组织都会产生淋巴细胞,提取的淋巴细胞不一定有抗肿瘤活性,即便有抗肿瘤活性患者也不一定能等待8周的时间以扩充培养这些淋巴细胞。因此,尽管有高达50%的治疗响应率,TIL疗法没能获得更广泛的应用。
这些限制促使研究人员寻求具有更广泛意义的T细胞。TIL疗法前后治疗数百例黑色素瘤患者的过程中,研究人员发现不同患者的TIL同样可以识别一些肿瘤细胞高表达抗原如MART-1、gp100等。基于这些发现,针对这些特定抗原的T细胞将具有潜在的治疗效果。这些尝试,将T细胞疗法推向靶向时代和重组改造时代。
TCR-T 疗法
Steven Rosenberg研究组选取了一个黑色素瘤患者的2个TIL细胞克隆DMF4、DMF5。这两种细胞系都对MART-1/HLAA*02(A2)有亲和力。患者的外周血T细胞被收集起来,并通过反转录病毒导入DMF4的TCR基因。这种方法避免了TIL复杂的分离过程,初步临床试验结果在2006年发表,12个黑色素瘤患者中有2位患者有治疗响应。尽管响应率远低于TIL疗法,但初次证实了基因改造的T细胞具有治疗效果。

TCR亲和力
TCR的亲和力是否是一个重要因素呢?由于DMF4的TCR对于MART-1的亲和力比较低,高亲和力的DMF5-TCR进行了又一项临床试验。治疗响应率达到30%(6/20),当然由于患者数少,也不能明确说亲和力高的TCR一定有更好的疗效。同时要注意,DMF5-TCR的毒性更大,出现了视力、听力、皮肤毒性。与这些部位正常组织表达的MART-1相关。

适应症拓展
继MART-1靶点的TCR-T疗法后,针对其他适应症的CEA、NY-ESO-1、MAGE靶点的TCR-T疗法陆续进入临床研究。Robbins等人开发的靶向NY-ESO-1的TCR-T疗法先后用于转移性黑色素瘤和滑液细胞瘤。治疗响应率分别为55%(11/20)和61%(11/18)。在宾大,“六爷”(Carl H June)研究组开发的靶向NY-ESO-1的TCR-T疗法用于多发性骨髓瘤,治疗响应率达到80%(16/20)。
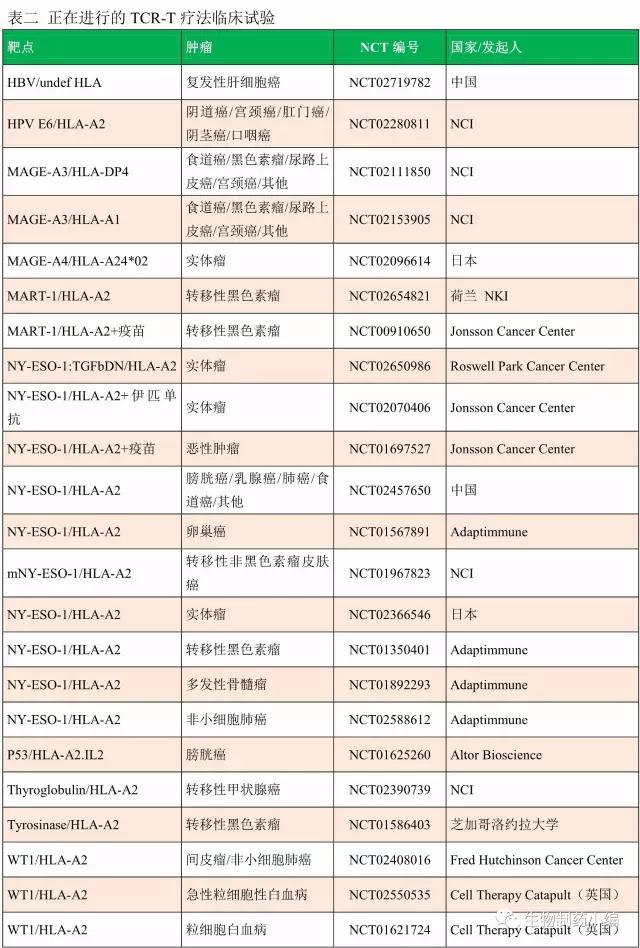
截止到2016年末,TCR-T疗法已经陆续被应用于多种适应症的临床研究:包括是到期、黑色素瘤、膀胱癌、肺癌、滑液细胞瘤等。这些正在进行的临床试验统计如下表。
精细的平衡
NCI 进行的靶向CEA的TCR-T疗法临床研究,3个病人有1例治疗响应,但3人都出现了严重的炎症反应-大肠炎。可能是由于大肠正常组织也表达CEA。
靶向MAGE的TCR-T疗法则有3项已完成的临床研究,如表一所示。NCI进行的靶向MAGE-A3的临床研究,有3位患者出现精神状态改变,其中2人陷入昏迷最终死亡。尽管这项研究中TCR是通过响应MAGE-A3呈递得到的,但已知MAGE-A9与MAGE-A12也有交叉反应活性。死后病理检查显示脑部大量T细胞浸润,同时证实脑部正常组织表达MAGE-A12,所以这个副作用很可能与此相关。
超生理状态TCR亲和力的风险
宾大进行一项靶向MAGE-A3的TCR-T疗法,用于治疗2例多发性骨髓瘤和1例黑色素瘤。TCR经过筛选,提高了亲和力。开始接受治疗的2例患者出现了心源性的休克并死亡。病理结果发现T细胞大量浸润导致心肌死亡坏死,而心脏组织是不表达MAGE-A3的。随后通过心肌细胞培养发现存在与MAGE-A3 TCR的交叉反应。进一步研究发现罪魁祸首是肌联蛋白-Titin,其产生了类似于MAGE-A3的多肽。这个案例提醒我们,TCR亲和力提高存在脱靶的风险,TCR-T疗法的应用要更加小心。
非自身抗原
除了自身抗原,也有研究人员开始尝试将TCR-T疗法用于外源抗原,如HPV的病毒抗原等。
CAR-T 疗法
TCR-T疗法展示了一定的治疗潜力,但仍有诸多限制,如组织相容性抗原配型、抗原需要呈递到细胞表面等。CAR-T疗法的出现大大拓展了T细胞疗法的应用范围。
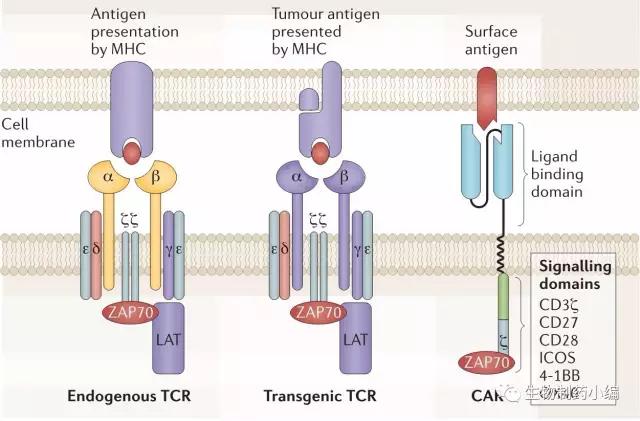
三代CAR的发展
CAR-T疗法的概念最早来自于Zelig Eshhar教授(以色列人,德国洪堡大学教授)。
Zelig Eshhar提出将抗体的轻重链连接到T细胞表面TCR的恒定区上,随后又将scFv替换轻重链,避免了多次重复的转基因。这就是第一代CAR-T疗法,随后陆续应用到临床上。
然而这些早期的临床研究没有获得理想的效果,响应率不佳,而且在靶向CAIX的CAR-T疗法中,出现了胆源性毒性的副作用,意味着CAR-T存在作用于正常组织中靶标引起毒性的风险。
CAR-T疗法的第一个积极临床结果于2008年公布,位于休斯敦的Baylor医学院的Malcolm Brenner研究组,靶向GD2的CAR-T疗法,尽管24小时血液中CAR-T细胞含量不足0.1%,仍使得11名儿科成神经细胞瘤患者中的3人完全缓解。随之而来的一个主要问题是如何保持CAR-T细胞的长期存活。
二代CAR-T引入了共刺激信号4-1BB或CD28,前者通过上调Bcl-xL延长T细胞的存活期,后者可以增强T细胞响应的效价。三代CAR-T引入2个以上的共刺激信号。
第一个三代CAR-T的临床研究为靶向HER2的CAR-T疗法,适应症为转移性黑色素瘤(表二)。HER2靶点在单抗领域已经成功应用多年,赫赛汀成功治疗超过40万名女性乳腺癌患者,表现出很小的毒性。基于这些经验,NCI选择将靶向HER2的scFv应用到CAR-T疗法上,用于治疗HER2+ 黑色素瘤。首例患者接受了高浓度的CAR-T细胞:1*1011个细胞。患者接受治疗后,几分钟后就表现极为痛苦,很快陷入昏迷,X光显示严重的费浸润。医生给予高剂量激素敢于,患者仍在5天后死亡。随后发现患者全身遍在CAR-T细胞,肺部最为严重。进一步分析肺部上皮细胞表达HER2,可能是导致肺部T细胞浸润引发死亡的主要原因。
CD19:成功的故事
HER2 CAR-T致患者死亡的案例对于CAR-T靶点选择产生了巨大的影响。CAR-T的靶标选择更加谨慎,科学家希望找到只在肿瘤细胞表达的靶标。这些尝试给了CD19、CD20发挥作用的机会,这是B细胞的两种分化抗原。第一个被尝试的是CD20,不过没有表现出明显的疗效,紧接着就是CD19的登场,CAR-T的光芒注定开始闪耀了。
2007、2008、2009年,Michel Sadelain(Baylor)、Carl H June(宾大)和Steven Rosenberg(NCI)研究组分别报道了CD19 CAR-T的临床前研究结果。2010年,Steven Rosenberg研究组的James Kochenderfer发表了CD19 CAR-T初步临床研究的结果,这项研究是基于CD28共刺激信号的二代CAR-T疗法,用于治疗晚期滤泡淋巴瘤(FL)。这项研究最后由8名患者参与,6名患者出现缓解。5名患者接受治疗后CAR-T在PBMC中含量超过1%,10天后达到峰值,一个月后含量回落到0.01%以下。
2011年,宾大的Carl H June教授发表了一例基于4-1BB共刺激信号、靶向CD19的二代CAR-T治疗案例,适应症为慢性粒细胞性白血病(CLL)。患者完全缓解,同时由于细胞因子风暴有发热症状。CAR-T的疗效持续达8周之久,有趣的是,患者接受的CAR-T细胞只有1.42*107个,比之前常用的剂量(109~1011)低了2-3个数量级。
同样在2011年,Renier Brentjens和Michel Sadelain(Baylor)发表了基于CD28共刺激信号、靶向CD19的二代CAR-T疗法,患者包括慢性粒细胞性白血病(CLL)和急性粒细胞性白血病(ALL),治疗剂量是107个/kg体重。大部分患者在接受治疗24h内出现发热,多数是暂时性的,只有1位患者持续发热最终死亡。死亡原因不明,但可能与之前已存在的脓毒症有关。
1例CLL患者出现缓解,疗效维持6个月;1例ALL患者出现缓解,但后来进行了骨髓移植治疗排除出试验。值得注意的是,接受治疗2周后,血液中都检测不到CAR-T细胞存在。
看到CAR-T的成功,更大规模的临床试验在FL、CLL、ALL及其他B细胞相关的恶性肿瘤患者中开展。这其中尤其值得注意的是多发性骨髓瘤的成功研究。
尽管多发性骨髓瘤(MM)被认为是一种B细胞疾病,但通常认为这是一种完全分化的、CD19阴性的B细胞疾病。2015年,Carl H June教授研究组的Alfred Garfall 和 Edward Stadtmauer发表了1例多发性骨髓瘤患者接受基于4-1BB共刺激信号、靶向CD19的CAR-T治疗的案例。这名患者是以为43岁的女士,经过9种化疗治疗和干细胞移植治疗,接受CAR-T治疗的时候,她的骨髓95% MM,99.95%的B细胞是CD19阴性的。CAR-T治疗剂量是5*107个,100天后骨髓中肿瘤细胞完全消失。科学家猜想可能0.05%的CD19阳性B细胞具有干细胞性质,是肿瘤细胞自我更新的基础。因此靶向CD19的CAR-T疗法可以治疗多发性骨髓瘤。
CD19之外的血液肿瘤靶点
尽管CD19 CAR-T已经表现了颠覆性的进展,仍有一些患者出现CD19靶标丢失以及治疗后复发,因此仍有必要寻找新的血液肿瘤靶点。靶向CD138、BCMA治疗骨髓瘤,靶向CD33、CD123治疗急性粒细胞性白血病(AML)的CAR-T疗法处在临床研究阶段。
双刃剑
活化的T细胞会产生大量的细胞因子:干扰素α、干扰素γ、IL-1、IL-2、IL-6、IL-8等。这些细胞因子会引起各种身体反应:发热、低血压、募集和激活更多免疫细胞导致更坏的后果甚至死亡。这种情况被称为细胞因子风暴(Cytokine release syndrome, CRS)。
Emily Whitehead是第一例接受CAR-T治疗的儿科ALL患者,宾大的CAR-T临床试验将Emily的白血病完全治愈。Emily当时处于白血病末期(ALL),接受CAR-T治疗四天后,Emily发了高烧,血压快速下降危及生命,第5天住进ICU。科学家和医生团队们不知道如何治疗,因为不知道原因何在。他们连夜测定了Emily体内细胞因子的水平,发现很多细胞因子都升高,IL-6升高幅度最大。医生讨论后给Emily注射了脱利珠单抗,一种IL-6R抗体药物。几乎是立刻,Emily的血压上升,退烧,其他症状也都回复正常。如今,Emily已经11岁,是一个完全健康的儿童。
还有很多情况下,细胞因子风暴无法有效处理,需要科学家对CRS进行更深入的研究和干预。如Juno领先的CAR-T疗法JACR015在2015年出现2例脑水肿死亡案例,这种情况下更难处理,如脱利珠单抗无法突破血脑屏障来干预脑部的副作用。
大胆探索“无人区”
CAR-T疗法在白血病领域的成功激发了大药企的兴趣,他们投入大量资金与研究机构合作推动CAR-T的临床研究。2013年,Fred Hutchinson、纪念斯隆・凯特琳癌症中心和西雅图儿童医院的科学家联手成立了Juno。宾大携手诺华开发CAR-T疗法,Kite则与NCI合作。礼来、葛兰素史克、强生、默克通过投资介入CAR-T领域。其他的CAR-T研发型企业包括BlueBird、Bellicum、Cellectis等,后文将一一介绍其技术特点。
CAR-T疗法在实体瘤领域遇到了很多困难,一度使得人们认为CAR-T不适用于实体瘤。如表二所示,目前二代/三代CAR-T疗法仅有2个案例研究和1项19人的临床研究。其中唯一的三代CAR-T实体瘤应用是由Steven Rosenberg's(NCI)研究组来进行的,治疗剂量为107个靶向HER2的CAR-T细胞,患者为复发性转移性黑色素瘤,可以患者由于正常组织靶点介导的严重副作用死亡。
另一个临床研究是靶向HER2的二代CAR-T疗法,由Baylor进行,入组19名复发性转移性肉瘤患者。该项研究中剂量使用更为谨慎,为104~108个,最高剂量人比NCI的案例低3个数量级。尽管没有副作用,但该研究也没能显示治疗效果。
首个靶向不同抗原(mesothelin,间皮素)的二代CAR-T来自宾大,用于治疗2例患者:1例恶性胸膜间皮瘤、1例转移性胰腺癌。尽管没有显示毒性,但只在恶性胸膜间皮瘤患者显示了暂时性的抗肿瘤效果。至今为止,其他经报道的实体瘤CAR-T疗法都是CD19 CAR-T成功前的第一代CAR-T疗法,他们几乎无效或者只有微弱的疗效。
自身抗原的尴尬
HER2 CAR-T疗法是一个生动的教训,提示我们T细胞的效价可以有多强,和单抗药物显示完全不同的安全风险。由于肿瘤细胞来自正常细胞,很难找到只在肿瘤细胞表达而在正常细胞完全不表达的靶点。正如已经尝试过的MART-1、gp100、CEA等一度认为是肿瘤特异性的,最后发现在正常组织也会有表达。
容易摘的果实
多形性成胶质细胞瘤(glioblastomamultiforme)的生存期只有15个月,三分之一的肿瘤细胞表达突变的肿瘤特异性抗原,这样靶向EGFRvIII的CAR-T疗法就成为一种理想的选择。因为EGFRvIII是一种肿瘤特异性的突变蛋白,正常细胞不可能表达,但不能完全避免EGFR与EGFRvIII的交叉活性反应。提高安全性的主要任务就是筛选对EGFRvIII高活性、对EGFR低亲和力的scFv。
宾大的Carl H June研究组开发了基于4-1BB共刺激信号、靶向EGFRvIII的CAR-T疗法,用于治疗多形性成胶质细胞瘤;NCI的Steven Rosenberg研究组开发了基于4-1BB和CD28共刺激限号、靶向EGFRvIII的CAR-T疗法,用于治疗晚期神经胶质瘤;杜克大学也开发了靶向EGFRvIII的CAR-T疗法,用于治疗多形性成胶质细胞瘤。具体见上表。
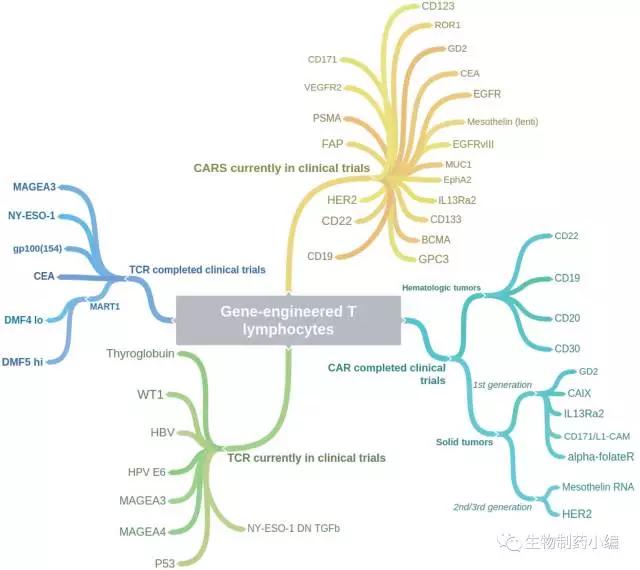
▲TCR-T疗法、CAR-T疗法临床研究一览
IL13Rα2是一种肿瘤特异性的靶标,针对这个靶点的CAR-T疗法经过十数年的研究。希望之城国家医疗中心(city of hope)的Michael Jensen研究组做了大量靶向IL13Rα2的研究工作。该研究组没有利用scFv,而是利用重组IL13(Zetakine)来靶向IL13Rα2。2015年,该研究组报道了临床研究结果:他们招募了13例GBM患者入组,不幸的是,DNA质粒电转、筛选、扩充培养耗费了3-4个月的时间,最终只有3位患者来得及接受CAR-T治疗。由于采取了肿瘤切除术,不确定治疗的效果,3位患者也在治疗一年内先后死亡。
再次探究自身抗原
理论上一些肿瘤靶标蛋白的表达会大幅上调,与正常组织存在很大差别,可以作为CAR-T的治疗靶点。一些靶向mesothelin、cMet、MUC1、GD2、EphA2、EGFR、CD171和CD133的CAR-T疗法正处在一期临床评价安全性的研究中。另外还有一些针对非肿瘤特异性表达、但在肿瘤微环境中特异性存在的靶点如FAP、VEGFR2的CAR-T疗法也在研究过程中。
“金发姑娘原则”
免疫系统本质上是一种平衡态,针对癌症进行免疫治疗一样要谨慎的平衡安全性与有效性。对于TCR-T疗法,只有靶标达到一定浓度,才能激活TCR下游信号。而CAR则不然。这是由于两者的作用方式不同,TCR:MHC-Peptide的相互作用一般在μmol级别,而scFv与表位的相互作用一般在nmol级别。如前文所述,NCI进行的MART-1 TCR-T疗法中,高亲和力的DMF5 TCR治疗响应率为30%,但毒性更强;低亲和力的DMF4 TCR治疗响应率为13%,但没有表现出毒性。
scFv与表位的亲和力也会因案例而异,但一般比TCR与MHC-peptide的亲和力高3个数量级。如宾大靶向EGFRvIII的scfv亲和力为101nM,而NCI靶向EGFRvIII的scFv亲和力为0.58nM。2015年,宾大的Yangbing Zhao教授和MD Anderson Cancer Center的Laurence Cooper教授(2015年任Ziopharm的CEO)在Cancer Research同一期发表了文章,研究内容都是引入突变到anti-HER2 scFv进行亲和力改造,进而在体外和小鼠体内研究改造对CAR-T造成的影响。有趣的是,两者都发现了亲和力的“sweet spot”,改造后只识别肿瘤细胞的高表达抗原,而不识别正常细胞的低表达抗原。这项研究成果被Baylor的临床研究证实:改造后的靶向不同表位的HER2 CAR-T在19例患者治疗中没有发现毒性。
CAR-T 疗法的毒性控制
RNA CAR
首个HER2 CAR-T疗法造成的死亡是的研究人员更为谨慎,一种控制安全性的策略是控制CAR-T细胞的暴露时间。宾大的Carl H June研究组开发了一种靶向间皮素的CAR RNA疗法,将RNA通过电转化导入T细胞,这样CAR 蛋白只会表达7天左右的时间。但这种方法过于复杂,而且通常需要连续几次的注射才有可能看到治疗效果。
给药途径
另一种减轻毒性的方法是肿瘤组织内注射,但这种方法只适合尚未发生转移、只分布在特定部位的肿瘤。这种方法比较适合GBM这种脑瘤,这样T细胞就不太会透过血脑屏障进入全身,避免发生更多副作用。2016年12月29日,新英格兰医学杂质发表了Michael Jessen研究组的成果,1位50岁的胶质母细胞瘤患者接受局部注射IL13Rα2 CAR-T的治疗后,取得良好进展。
▲IL13Rα2 CAR-T治疗后局部肿瘤的控制
降低剂量
Baylor试图通过降低剂量来解决毒性问题,鉴于NCI 的HER2 CART高剂量(1011个)导致患者死亡,Baylor 在NCT02442297种的剂量降低至107~108个,另一项治疗HER2阳性的恶性肿瘤试验(Bucket trial)剂量最低至104个。Baylor认为通过筛选病毒特异性的记忆T细胞会更有利于安全性,不过这种方法耗时更长更繁琐,关于细胞的筛选对安全性的影响也没有定论。
细胞自杀系统
另一种限制毒性的机制是scFv的免疫原性,导致其清除。NCI的鼠源gp-100 TCR显示确实产生了人抗鼠抗体(HAMA)。但这个机制不能解释CD19 CAR-T疗法中CAR-T细胞的衰减,因为该疗法在清除血液里的肿瘤细胞的同时也会清除正常的B细胞。血液里所有B细胞都被清除,也就无法产生抗体,自然无法清除CAR-T细胞。然而在实体瘤的CAR-T疗法研究中,免疫原性又称为一个治疗障碍,CAR-T疗法已经有许多人源化以减少免疫原性的尝试。这些矛盾的现象需要进一步深入研究。
科学家更多尝试利用非免疫原性的方法来控制CAR-T细胞的活性,传统的方法是使用大量激素,但有时候激素不足以控制细胞因子风暴。许多研究团队进而开发了CAR-T的开关系统。如MSKCC开发的一种CAR-T疗法开关,在CAR-T细胞同时包含一种Caspase9蛋白,这种蛋白只有在二聚体情况下才有活性,而二聚体的形成是某种特定的小分子药物介导的。使用这种药物后,Caspase 9蛋白会二聚化,活化后的Caspase 9蛋白会介导CAR-T下包的凋亡。从而达到作为CAR-T疗法开关的目的,这种开关设计还有很多,后文CAR-T企业介绍中会涉及到多种不同的CAR-T开关。
T细胞疗法的未来方向
免疫检点抑制剂、T细胞疗法是肿瘤免疫疗法的两大突破性进展。T细胞疗法中,刺激性信号4-1BB、CD28、OX-40、CD27、ICOS等已经被正和岛CAR-T疗法中,增强T细胞活性,延长存活周期。另一方面,针对抑制性信号的免疫检点抑制剂抗体如PD-1/PD-L1抗体已经取得了许多突破性进展。CAR-T、TCR-T疗法在某些患者没能产生治疗响应,其区别也仅仅是T细胞对肿瘤细胞不响应,不能产生IFN-γ等细胞因子。由此猜想可能是抑制性信号发挥了抑制T细胞响应的作用。2016年9月,Carl H June研究组发表了PD-1抗体与CAR-T联用的研究,PD-1抗体可以增强CAR-T疗法的疗效。
100种实体瘤本质上就是100种不同的疾病,这些差异性给T细胞疗法带来许多挑战。需要更多的基础研究以探索发病机制,如胰腺癌的屏障来自于基底组织,GBM则分泌TGF和T细胞抑制因子。幸运的是,资本的涌入极大促进了T细胞疗法的发展,传统化疗、放疗及新兴的免疫检点抑制剂,联用的协同效应给癌症治疗带来更多选择。未来的方向还不得而知,但免疫治疗的前景一定是光明的。
T 细胞疗法研发企业
宾夕法尼亚大学、美国癌症研究院(NCI)、Fred Hutchinson癌症研究中心、纪念斯隆・凯特琳癌症中心、和西雅图儿童医院等是最早开展CAR-T细胞疗法的研究机构。2013年,Fred Hutchinson、纪念斯隆・凯特琳癌症中心和西雅图儿童医院的科学家联手成立了Juno。宾大则携手诺华开发CAR-T疗法。Kite则与NCI合作,从而形成了三巨头鼎立的局面。除此外,还有Bluebird、Celletis、Bellicum等多家企业布局CAR-T疗法。
附表 CAR-T、TCR-T疗法研发企业
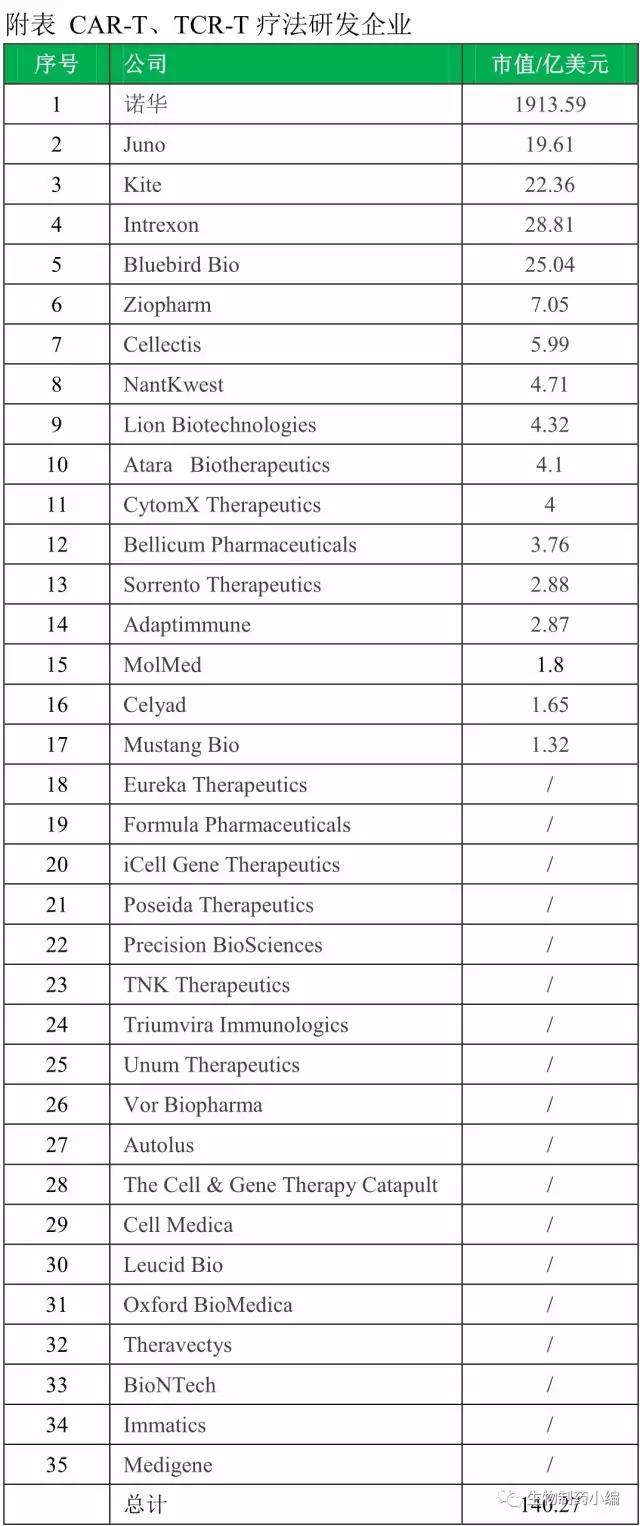
除了CAR-T、TCR-T细胞疗法的研发企业外,大药企也对这个新兴领域虎视眈眈。前有诺华与宾大合作,后有安进成立自己的CAR-T疗法研发企业Atara,其他大企业则通过合作形式纷纷布局CAR-T/TCR-T疗法领域。
1
Juno
Juno在CAR-T细胞疗法领域与诺华、Kite处在第一梯队,并积极开展多项研发合作,保持技术领先及策略的灵活选择空间。Juno与纪念斯隆・凯瑟琳癌症研究中心(MSKCC,JACR015)、Fred Hutchison癌症研究中心(FHCRC,JACR014)、西雅图癌症研究所(SCRI,JACR017)积极开展合作,并在近两年先后收购了Stage Cell、AbVitro、Redox Therapies三家生物科技公司,最近则与张峰创办的Editas签订合作协议,Juno一系列密集布局旨在加强CAR-T领域的布局。中国市场方面,Juno与药明康德成立合资公司,共同在中国推进其细胞疗法项目的开发。
2016年7月6日,JCAR015在针对成人复发或难治性B细胞急性淋巴细胞白血病的Ⅱ期临床试验中导致2例患者脑水肿死亡而被叫停,Juno在7月8日前递交修订材料,7月12日,FDA审核后排出JCAR015产品本身问题,许可JACR015继续临床试验。FDA快速反应的积极态度,将该事件的负面影响降到最低。11月23日,Juno再次宣布暂停JACR015的临床研究,股价应声下滑30%。
产品布局方面,第一梯队为靶向CD19的CAR-T疗法:JACR015、JACR017、JACR014。JACR015在纪念斯隆・凯特琳癌症研究中心开发,采用CD28作为共刺激因子,采用细胞为CD3+ PBMC,适应症为ALL、NHL;JACR017在西雅图癌症研究所开发,采用4-1BB作为共刺激因子,采用细胞为固定比例的CD8+ T细胞/CD4+ T细胞;适应症为儿科ALL、NHL;JACR014在Fred Hutchison癌症研究中心开发,采用细胞为固定比例的CD8+ T细胞/CD4+ T细胞。
除此外,Juno积极开发升级版的CAR-T疗法:双特异性的CAR-T疗法。第二个特异性受体可以是激活型信号也可以是抑制性信号。以抑制性信号iCAR为例,设计为特异性识别健康组织中存在的靶标蛋白,如下图中的antigen B,癌症组织中,CAR识别antigen A杀伤癌细胞,正常组织中,antigen B结合iCAR,启动抑制信号,T细胞不会杀伤带有靶标antigen A的正常细胞。这样就提高了CAR-T疗法的特异性和安全性。
CD19之外,Juno也在积极开发其他靶点的CAR-T疗法,如CD22、WT1等靶点,以开发针对不同适应症的产品。CAR-T疗法之外,Juno同时开发TCR-T疗法。
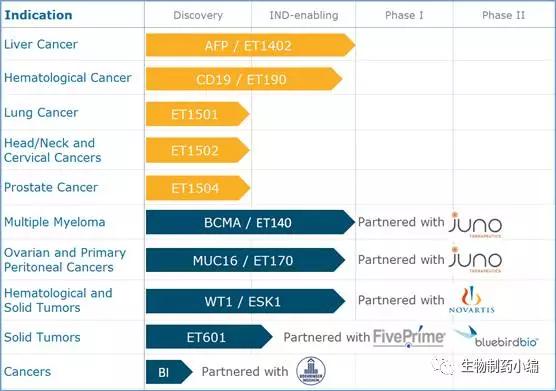
Juno pipeline
2
诺华
诺华的CAR-T技术源自宾夕法尼亚大学,前文已有具体阐述。2016年8月31日,诺华宣布解散细胞和与基因治疗部门,并入肿瘤研究部门。诺华宣诚CAR-T疗法的开发不收影响,但业界更倾向于相信诺华对CAR-T多少存在一些顾虑。诺华进展最快的CAR-T疗法为CTL019,属于第二代CAR-T疗法,胞内信号区共刺激信号为CD-3zeta和CD137。在2016年ASH会议上,诺华公布了CTL019二期临床数据,针对儿童和年轻人难治性复发性B-ALL的完全缓解率达到82%。副作用仍然严重,48%的患者出现了3级-4级的CRS,但没有出现治疗相关的死亡。15%的患者出现了3级神经毒性。
3
Kite
Kite Pharma的研发进度原本稍落后于Juno和诺华。2016年12月4日,Kite宣布其领先产品KTE-C19已经启动BLA滚动申报,适应症为不适合自体干细胞移植的复发性难治性B细胞非霍奇金淋巴瘤,从而后来居上。
根据2016年9月26日公布的KTE-C19的二期临床研究中期数据(ZUMA-1),疗效达到预期:弥漫性大B细胞淋巴瘤(DLBCL,51位患者)总体反应率ORR达到76%,完全缓解率CRR达到47%;转移滤泡性淋巴瘤(TFL,11名患者)总体反应率ORR达到91%,完全缓解率达到73%。Kite希望能在2017年上市该产品,尽管CMO仍保持谨慎态度,主要是KTE-C19仍存在一些严重的安全性问题。此外,KTE-C19的疗效持续时间也是一个问题,3个月后总响应率和完全缓解率都出现明显下降,但是否如一期临床研究一样,3个月后的有效率不再发生明显变化,尚不得而知。
Kite与Cell Design Labs合作,引入小分子开关到新一代CAR-T疗法中。
4
Adaptimmune
Adaptimmune的前身是Avidex,其技术源自牛津大学。2006年,Avidex被Medigene收购,2008年,Adaptimmune分拆出来成为独立公司,并与宾大达成技术合作协议。2014年于葛兰素史克达成合作协议,随后完成1.04亿美元的A轮融资。2015年5月,Adaptimmune在纳斯达克上市,募资1.76亿美元。
Adaptimmune通过改造TCR的CDR域,提高TCR与靶点蛋白的亲和力。技术实现途径包括:确认特异性的靶标,首先确认癌细胞呈递的多肽,然后筛选掉正常组织中呈递的多肽,验证该多肽在癌细胞表面呈递;确认靶标后,建立IP保护的TCR噬菌体展示库,通过IP保护的二硫键方法改造后的TCR更加稳定并可溶,从中筛选高亲和力高特异性的TCR;筛选的TCR通过IP保护的临床前安全性测试技术验证,保证最小的off-target效应、Cross-activity(正常组织活性)。
从病人体内分离CD4、CD8细胞后,进行上述基因的改造。改造后的T细胞通过DynaBeads® CD3/CD28 beads技术进行扩增,最后冻存备用。
基于上述技术平台,Adaptimmune开发了靶向NY-ESO、MAGE-A10等的TCR-T细胞疗法,并在2014年6就NY-ESOTCR-T项目与GSK签订了合作开发协议,协议总金额达3.5亿美元。
5
Atara Biotherapeutics
Atara由安进与风投公司凯鹏华盈于2012年联合创立,公司名字来自一位癌症患者。
Atara的技术来自纪念斯隆、凯特癌症研究中心,通过分裂健康志愿者的T细胞,进行扩增后用相应抗原处理活化T细胞,保存备用。使用的患者需要进行HLA匹配。
目前EBV-CTL、CMV-CTL处于二期临床研究阶段,WT1-CTL处于一期临床研究阶段。2015年2月,FDA授予EBV-CTL治疗利妥昔单抗难治性的EBV相关淋巴组织增生性疾病(EBV-PTLD)的突破疗法认定。
6
Bellicum Pharmaceuticals
Bellicum的一项核心技术CID是给细胞疗法加入了一个“开关”,通过小分子rimiducid来控制信号通路的开关。该技术可以作为安全开关,rimiducid诱导细胞凋亡(当细胞疗法出现毒性时使用);也可以作为活化开关,rimiducid诱导细胞更多的增殖(当细胞疗法作用不够强时使用)。细胞疗法一个很大的问题是个体差异大,剂量不好控制,有时候出现严重副作用,有时候又不够强起不到治疗效果,CID使得细胞疗法的应用更加灵活可控并且安全。
CID技术的实现途径:信号域使用特定的蛋白分子启动相应的信号转到途径。
安全开关:Caspase-9开关,Caspase-9是细胞凋亡的起始酶,通过活化Caspase-3等一系列信号转到,最终诱导细胞凋亡。
活化开关:MyD88/CD40开关,MyD88是一种应激反应信号蛋白,如在细胞因子、病毒侵袭时促使细胞通过活化or增殖应对刺激;CD40则是一种共刺激信号蛋白。MyD88、CD40的作用主要在树突细胞中研究较多,Bellicum则创新性应用到T细胞中。
CID技术可以应用到不同的细胞疗法:造血干细胞移植(HSCT)、CAR-T疗法、TCR-T疗法。Bellicum在此基础上开发了自己的TCR疗法技术CaspaCIDe和CAR-T疗法CIDeCAR、GoCAR-T。
Bellicum pipeline
CaspaCIDe
2016年8月4日,欧盟委员会授予BPX-501用于造血干细胞移植(HSCT)和激活剂rimiducid用于移植物抗宿主病(GVHD)治疗以孤儿药资格认定,今年早些时候,BPX-501和rimiducid以联合治疗获得美国食品药物管理局授予孤儿药地位。
CIDeCAR
GoCAR-T
7
Bluebird Bio
蓝色小鸟是一家专注开发基因治疗药物的生物制药企业,2013年Bluebird与新基签订协议,合作开发CAR-T疗法。两家公司后来收紧合作范围,重点开发靶向BCMA的CAR-T疗法bb2121,适应症为多发性骨髓瘤,目前处于一期临床研究阶段。新基的核心产品正是治疗多发性骨髓瘤的来那度胺,2015年销售额58亿美元,BCMA则是多发性骨髓瘤最为热门的新靶点。新基将热门技术CAR-T与BCMA结合,布局也是颇为考究。
8
CytomX Therapeutics
CytomX是一家抗体药物研发企业,其核心技术是Probody,通过融合一段多肽屏蔽抗体活性,linker则在肿瘤组织特异性的酶作用下断裂,释放有活性的抗体,提高抗体正常组织中靶产生的毒性。CytomX将该技术应用到CAR-NK技术中,建立了ProCAR-NK技术,相对于传统CAR-NK提高了病变组织特异性。
9
Eureka Therapeutics
Eureka成立于2006年,是由华人科学家刘诚等创办的公司,总部位于美国加州湾区,目前在北京设有分公司优瑞科。
Eukera的核心技术是开发针对细胞内靶点多肽(实际上是抗原处理后被MHC呈递到细胞表面的多肽)的抗体,即功能上类似于TCR的抗体。刘诚等还将该技术写进了springerlink 2015年出版的《Peptide Antibody》一书中,作为该书的第十七章:Generation of TCR-Like Antibodies Using Phage Display。Eukera与Juno等合作将该技术应用到CAR-T上,从而可以得到针对这些胞内靶标的CAR-T疗法。
10
Formula Pharmaceuticals
Formula原来是一家研发癌症疫苗的企业,2014年转变方向到CAR-NK疗法研究,使用的是嵌合抗原受体的C.I.K细胞,即CIK-CAR技术。从捐献者获得C.I.K细胞,使用非病毒法基因改造。


11
iCell Gene Therapeutics
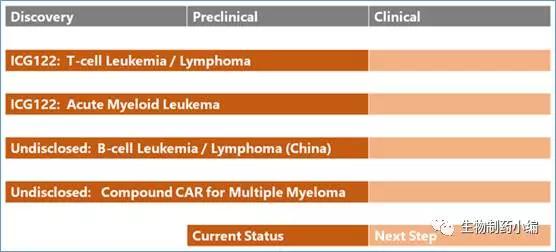
iCell Gene开发常规的CAR-T疗法,此处不多做介绍,进展最快的项目为靶向CD4的ICG122,FDA已经授予治疗PTCL的孤儿药资格。
12
Intrexon、Ziopharm
这两家公司的技术都来自安德森癌症研究中心,该CAR-T疗法采用了非病毒转染系统“睡美人”(sleeping beauty,简称SB)技术。
应用睡美人技术的CAR-T疗法在临床上表现除了更好的效果,PFS的OS成本增加。

ZioPharm Pipeline
13
Lion Biotechnologies
Lion与NCI合作开发了TIL疗法技术平台,TIL来自于肿瘤组织分离的细胞,更适宜用于实体瘤的治疗,有其差异化优势。
Lion 围绕TIL疗法进行了升级:对TIL进行目的基因的改造,以求提高杀伤活性并寻求专利保护。Lion的lead产品LN-144处在二期临床研究阶段,适应症为黑色素瘤,Lion同时将TIL疗法与PD-1抗体等展开联合治疗的临床研究。
生产方面,Lion积极推进TIL疗法的商业化生产,并在2015年与药明康德达成协议,后者为Lion提供扩大的TIL产能。
14
Mustang Bio
Mustang Bio 成立于2015年,其细胞疗法与city of hope癌症研究中心合作开发,主持者为来自COH(city of hope)、针对CAR-T疗法做出开创性贡献的Stephen Forman 和Christine Brown博士。
Mustang Bio旗下有两款CAR-T疗法已经进入一期临床研究,靶向IL13Rα2的MB101(适应症为难治性恶性胶质瘤)和靶向CD123的MB102(适应症为复发性急性粒细胞白血病AML)。
GBM同类产品竞争格局:
CD123靶点产品竞争格局:
15
NantKwest
2015年7月27日,NantKwest上市,首日涨幅超过40%,市值一度达到30亿美元,仅次于Juno,这个当时只有11名员工的细胞疗法研发企业进入人们视野,其创始人为华裔医生黄馨祥(黄馨祥收购ConKwest后改名)。正如企业新的名字暗示的那样,NantKwest的主要技术为CAR-NK疗法。
NantKwest的NK细胞经过改造不表达杀上抑制受体(KIR),可以避免肿瘤细胞等的免疫逃逸。基于独特的工程化NK细胞,NantKwest开发了抗体介导的高亲和力HaNK技术平台和靶向CAR-NK疗法taNK技术平台。
HaNK技术平台:抗体药物的靶向性来源于Fab与抗原的特异性结合,结合后通过ADCC、CDC等机制杀伤靶细胞。ADCC是许多传统抗体药物的重要作用机制,ADCC的一个重要途径为NK细胞的杀伤作用,通过受体CD16来介导。但一般情况下,人NK细胞的高亲和力CD16只占20%左右,多数NK细胞的CD16是低亲和力的,导致抗体药物的ADCC活性较弱。NantKwset对aNK细胞进行进一步改造,表达高亲和力的CD16。这样HaNK细胞疗法与抗体药物联用时,大大提高抗体药物的活性。


taNK:taNK即为基于工程化NK细胞的CAR-NK疗法,通过CAR达到靶向性NK细胞疗法的目的。NantKwest进展最快的taNK项目为靶向HER2的CAR-NK,另有多个taNK项目处于不同研发阶段。
16
Poseida Therapeutics
Poseida从Transposagen拆分出来,后者与强生关于CAR-T疗法的合作也转移到Poseida。Poseida专注癌症、罕见病的基因疗法与CAR-T疗法的开发。Poseida拥有多项相关技术:piggyBacTM DNA Modification System, XTNTM TALEN和 NextGENTM CRISPR site-specific nucleases, 以及Footprint-FreeTM Gene Editing (FFGE)。
2015年12月,Poseida完成了A轮融资,目前商务产品进入临床研究。
17
Precision BioSciences
Precision Biosciences是一家专注基因编辑技术的公司,拥有基于归槽内切酶的ARCUS基因编辑技术平台。2015年5月完成2560万美元A轮融资,2016年3月Baxalta与Precision达成协议,合作开发肿瘤免疫疗法CAR-T疗法。
Precision寻求开发基于异体T细胞的CAR-T off-the-shelf疗法,便于更方便的生产和使用。
18
Sorrento Therapeutics
Sorrento也是由黄馨祥创立的生物制药公司。Sorrento布局领域广泛:生物类似药、肿瘤免疫抗体、细胞疗法、ADC等,其中生物类似药主要与张江生物合作,细胞疗法方面在2016年6月与三生药业在国内成立合资公司,三生药业以1000万美元取得51%股权。CAR-NK细胞疗法则与NantKwest合作开发。

19
TNK Therapeutics
Sorrento子公司,专注细胞疗法。
20
Triumvira Immunologics
Triumvira的技术来自加拿大麦克马斯特大学Jonathan Bramson博士的实验室,一种基于TAC技术平台的CAR-T疗法。
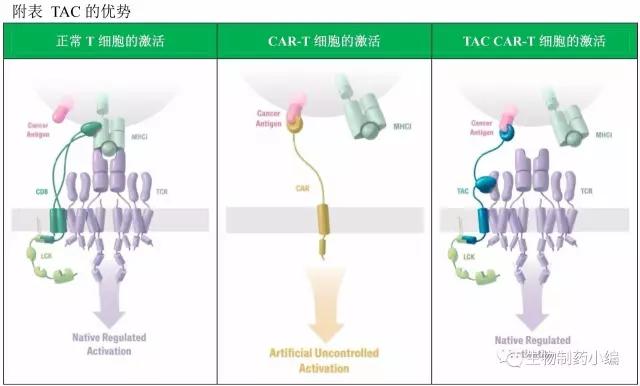
TAC的设计包含三部分:第一部分为胞外的抗原结合域(抗体片段或者DARPin等)、第二部分为胞外的anti-CD3 scFv、第三部分为跨膜的CD4 domain连接蛋白激酶LCK。总体设计更类似于TCR,受体改造的结果是对T细胞的激活保持在正常的范围。
基于TAC的CAR-T的生产与常规CAR-T类似。
TAC的优势:TAC受体的设计保留的TCR complex的功能,T细胞的激活与正常T细胞的激活是类似的,相当于加了一个阻尼,避免过度激活。
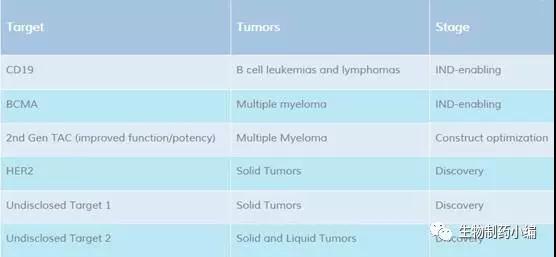
目前Triumvira 靶向CD19、BCMA的项目已经准备申报IND,另有多个项目处于前期研究阶段。
21
Unum Therapeutics
Unum开发了ACTR细胞疗法,该技术独具特色:靶向抗体药物而非抗原,需要与抗体药物联用。这有点类似于NantKwest的HaNK细胞疗法。2015年6月Unum完成6500万美元的B轮融资。
22
Vor Biopharma
Vor Biopharma成立于2016年5月,由PureTech发起创立,核心技术CAR-T疗法来自哥伦比亚大学医学院助理教授Siddhartha Mukherjee的实验室,Siddhartha Mukherjee是著名科普书籍《众病之王:癌症传》的作者。
23
Autolus
Autolus是从伦敦大学学院剥离出来的生物技术公司,主要开发新一代CAR-T疗法,2016年3月完成4000万欧元的B轮融资。Autolus的CEO Christian Itin博士从事肿瘤免疫研究多年,任职Micromet CEO期间主持开发了双特异性抗体Blincyto(CD19*CD3),如今开发CAR-T疗法也是水到渠成的事。
Autolus旨在开发新一代CAR-T疗法,解决目前CAR-T疗法安全性问题以及更多肿瘤适应症的问题。
24
The Cell & Gene Therapy Catapult
专注开发细胞疗法,是一家非营利机构,旨在成为联系工业界与学术界的转化桥梁。

25
Cell Medica
Cell Medica的lead项目均为上一代细胞疗法(T-CelleratorTM),CAR-T、TCR-T疗法尚处在早期阶段。


26
Leucid Bio
Leucid Bio是从英国国王学院剥离出来的生物科技公司,开发的CAR-T疗法已经启动一期临床研究(NCT01818323),但目前仍未筹集到资金,仍处在和投资者谈判的过程中。
27
Oxford BioMedica
Oxford Biomedica拥有专利保护的LentiVector基因改造技术平台,基于此开发了多种基因疗法产品。Oxford Biomedica自己并不开发CAR-T疗法,但在2013年,诺华以1400万美元的代价换取Oxford Biomedica为其CTL019项目生产表达CTL019的LentiVector质粒。
28
Cellectis
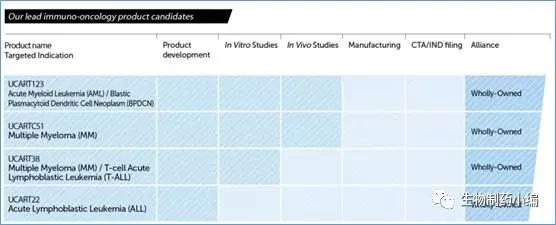
Cellectis位于法国巴黎,成立于1999年,名副其实的老牌生物科技公司。Cellectis利用TALEN技术进行基因改造,采用异体T细胞的CAR-T疗法,先后与辉瑞、施维雅达成合作开发协议。2015年,启动UCART19项目的一期临床研究。在研项目还有靶向CD123、CD38、CD22的CAR-T疗法。
2015年11月,Cellectis完成UCART19项目的三批GMP生产,股票应声大涨20%。由于Cellectis采用异体T细胞,其CAR-T疗法更容易标准化和灵活应用给更广泛的患者人群。因此,顺利实现GMP生产意味着其产品离上市又近一步。
29
Celyad
Celyad是一家比利时的制药企业,成立于2007年,2015年收购Oncyte获得NKR-2T细胞疗法,6月19日登陆纳斯达克。NKR-2 T细胞疗法能够识别多种肿瘤抗原,并使T细胞表达自然杀伤细胞受体NKG2D。当NKG2D与肿瘤表面配体结合时,就能杀死肿瘤细胞。Cylyad同时开发基于NKR-2T的自体/异体疗法,自体疗法已经进入一期临床研究阶段。
30
MolMed
2015年4月,MolMed从San Raffaele Hospital收购靶向CD44V6的CAR-T疗法,CD44V6在血液癌症和一些实体瘤中均有表达,60%的AML和90%的MM表达CD44V6。
31
Theravectys
THERAVECTYS是巴斯德研究所(Pasteur Institute)衍生的一家私营、全面整合型发现与临床开发生物技术公司。公司发挥其在慢病毒载体领域超过15年的基础研究的优势,已获得巴斯德研究所知识产权的全球独家授权。THERAVECTYS在其慢病毒载体技术平台的基础上,开发了用于抗击癌症和感染性疾病的治疗性疫苗和免疫治疗药物,包括一种专利的区分性CAR T细胞技术平台。
32
BioNTech
BioNtech位于德国美因茨,专注MRNA药物、细胞疗法、基因疗法等,深耕肿瘤免疫领域
33
Immatics
Immatics是一家癌症疫苗研发企业,Pipeliner如下
34
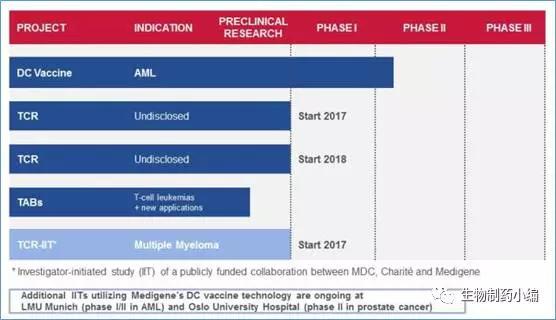
Medigene
Medigene是一家德国生物技术公司,成立于1994年。近年来开始开发T细胞疗法,相关Pipeliner如下
35
Bioalta
Bioatla是一家位于圣地亚哥的生物技术公司,开发了条件活化生物大分子(Conditonally Active Biologics)技术平台。这种技术得到的大分子如抗体只有在特定条件下(如肿瘤微环境的条件)才会活化,从而提高了安全性。
2015年4月,未名集团投资Bioatla成为其最大机构股东。2017年1月6日,Bioatla宣布与未名集团投资的另一家公司F1 Oncology合作开发基于CAB的CAR-T疗法,并计划在2017年启动首个实体瘤CAR-T临床试验。
此外还有TILT Biotherapeutics、Vira therapeutics等布局CAR-T、TCR-T疗法的企业,因公开信息有限,这里不再一一介绍。
小编总结
免疫检点抑制剂、CAR-T疗法的兴起标志着医学已经发展到非常深入的地步,从化疗的“干预”回归到人体自身免疫系统的“平衡”,不得不慨叹免疫系统的复杂。多数疾病最终都归因于免疫系统的失衡,如何调节失衡的免疫系统以对抗疾病,已经在不知不觉中成为一种至关重要的手段。“金发姑娘原则”也好、阴阳调和理论也罢,本质上都是对免疫系统调节的一种哲学阐释,利用自身免疫系统以对抗疾病,将是一条没有终点但充满前景的发展之路。
目前CAR-T疗法动辄数十万美元的价格不是普通患者能够承受的,工业界仍需在标准化、控制成本等方面持续努力。中国企业将在这一过程中扮演重要角色,一方面有博生吉、西比曼等立足国内开发CAR-T疗法的公司,一方面有药明康德在全球CAR-T疗法中提供生产外包服务。中国市场的高度价格敏感性将促使企业不断谋求降低CAR-T疗法成本,最大限度提高药物可及性。
参考资料
Engineered T cells the promise and challenges of cancer immunotherapy(2016);
CAR therapy= the CD19 paradigm(2016);
CAR T-cell immunotherapy:The path from the by-road to the frreway(2016);
CAR-modified T-cell therapy for cancer:an updated review(2016);
Driving gene-engineered T cell immunotherapy of cancer(2016);
PD-1 Blockade Modulates Chimeric Antigen Receptor (CAR) Modified T Cells and Induces Tumor Regression: Refueling the CAR。
温馨提示:
本文章出于传递更多信息之目的,仅供读者参考,并不意味着本站赞同其观点或证实其描述,一切诊断和治疗请遵从医生的指导。如果还有其他疑问,您可以拨打免费长途电话400-6000-838进行咨询,或者直接联系我们。
- 没有相关文章